在生物制品尤其是细胞与基因治疗(CGT)产品快速发展的今天,支原体污染控制与快速检测已成为保障产品质量和实现临床可及性的关键瓶颈。湖州申科生物技术股份有限公司基于其 MycoSHENTEK® 技术平台,构建了一套覆盖方法验证、复杂基质检测、全自动快速检测的完整支原体qPCR(荧光探针法)检测解决方案,全面响应行业从研发到放行的迫切需求。
一、应对行业核心挑战:为何需要支原体qPCR快检?
传统支原体检测方法(培养法需28天,指示细胞法需7-14天)的漫长周期,与CGT产品短货架期、快速放行的要求严重冲突。对于已制备完成的CAR-T等产品,患者等待就绪,但长达数周的支原体检测成为放行的“卡脖子”环节。此外,新型生物制品(如高浓度细胞悬液、含血清白蛋白的制剂、全血、质粒等)的复杂基质,也对检测方法的耐受性和准确性提出了更高要求。
核酸扩增技术(NAT),特别是qPCR方法,以其高灵敏度、高特异性、检测快速(仅需数小时)的优势,成为理想的替代方案。全球主要药典(如EP, USP, JP)均已认可或收录NAT方法,为其合规应用铺平了道路。
二、湖州申科MycoSHENTEK® qPCR检测体系的核心构成
湖州申科的解决方案并非单一试剂盒,而是一个包含标准品、试剂盒、自动化设备及技术服务的完整生态系统。
1.标准品与验证基础:确保LOD“真实可信”
支原体qPCR检测的可靠性,首要取决于验证用菌株的质量。检测限(LOD)的可靠性依赖于菌株的GC/CFU比值。若比值过高(如>10),检测信号可能主要来自死菌核酸,导致灵敏度被“虚假放大”。
支原体验证菌株:湖州申科提供口腔支原体、肺炎支原体、猪鼻支原体等药典优先推荐的标准菌株。这些菌株溯源至知名保藏机构,经培养法标定CFU,并经dPCR标定GC,确保GC/CFU比值可控(符合EP 2026新规<10的要求)。提供10 CFU/mL和100 CFU/mL两种浓度,直接用于方法灵敏度验证。
支原体DNA校准品:为质粒DNA,用于建立标准曲线,验证检测灵敏度和线性关系,操作方便且无生物安全风险。
2.检测试剂盒:历经验证,覆盖全面
湖州申科提供多代支原体qPCR检测试剂盒,均采用荧光探针法,并包含内部质控(IC)和阴阳性质控体系,防止假阴/假阳性。
高性能验证:试剂盒参照EP 2.6.7、JP XVII及中国药典<9201>要求完成了全面性能验证。验证数据显示,对10余种标准菌株(包括药典要求的和非药典的)在10 CFU/mL浓度下,检出率可达95%以上(如24/24),满足替代培养法(≤10 CFU/mL)和指示细胞法(≤100 CFU/mL)的灵敏度要求。
广谱覆盖:试剂盒引物探针设计覆盖近200种支原体、螺原体及无胆甾原体。
基质耐受性强:专门针对极端复杂基质进行了强化验证,包括10⁷个/mL的高密度细胞(Vero, 293T, CHO)、5%人血白蛋白、全血、1 mg/mL质粒等。验证数据表明,在这些基质中,对10 CFU/mL的支原体仍能保持高检出率。
快速版试剂盒:进一步优化流程,将从样本到结果的全程时间缩短至2.5小时,更适用于工艺过程实时监控和快速放行场景。
3.全自动检测系统:创新流程,杜绝污染
为解决传统qPCR操作步骤繁琐、易受气溶胶污染、对实验室环境和人员要求高的问题,湖州申科推出了全自动解决方案:AdvSHENTEK®外源因子全自动核酸检测分析系统+一体化支原体检测卡盒。
封闭设计:卡盒预分装所有试剂,仅加样一步需开盖,极大降低交叉污染风险。
“样本进,结果出”:系统集成核酸提取与qPCR扩增检测,自动完成并输出结果。
便捷高效:无需专业PCR实验室,在普通实验室环境即可操作。单次运行约2.5小时,4通道/16通道可独立运行不同项目,提升效率。
数据合规:系统具备三级权限管理、审计追踪功能,符合21 CFR Part 11等电子数据规范。
性能可靠:该系统同样经过严格验证,在复杂基质下检测限可达10 CFU/mL,满足药典要求。
三、 紧扣法规前沿:符合2026年EP新规要求
2026年4月1日,《欧洲药典》12.2更新了通则2.6.7 “支原体(MYCOPLASMAS)”,湖州申科的体系前瞻性地契合了这些新要求:
NAT地位提升:新EP将NAT正式列为与培养法、指示细胞法并列的三大核心方法之一。MycoSHENTEK®体系为此提供了成熟的技术选择。
验证要求量化:
① 灵敏度:明确替代培养法需≤10 CFU/mL,替代指示细胞法需≤100 CFU/mL。湖州申科试剂盒验证数据完全满足。
② 菌株要求:明确要求验证用活菌参考品的GC/CFU比值应<10。湖州申科的标准菌株制备与表征符合此标准。
③ 抑制物测试:新规强制要求NAT法进行抑制物测试。湖州申科在复杂基质下的全面验证数据,实质上完成了针对各类基质的抑制物评估。
取样策略:新规强调由于支原体可能附着于细胞,应同时检测细胞和上清液。湖州申科的提取试剂盒(磁珠法)能有效处理细胞悬液样本,确保细胞关联支原体的检出。AdvSHENTEK®外源因子全自动核酸检测分析系统可以实现支原体检测“样本进,结果出”的全样本量检测。
四、 全面的技术服务支持
湖州申科不仅提供产品,还提供配套的技术服务,助力企业完成方法变更和监管申报:
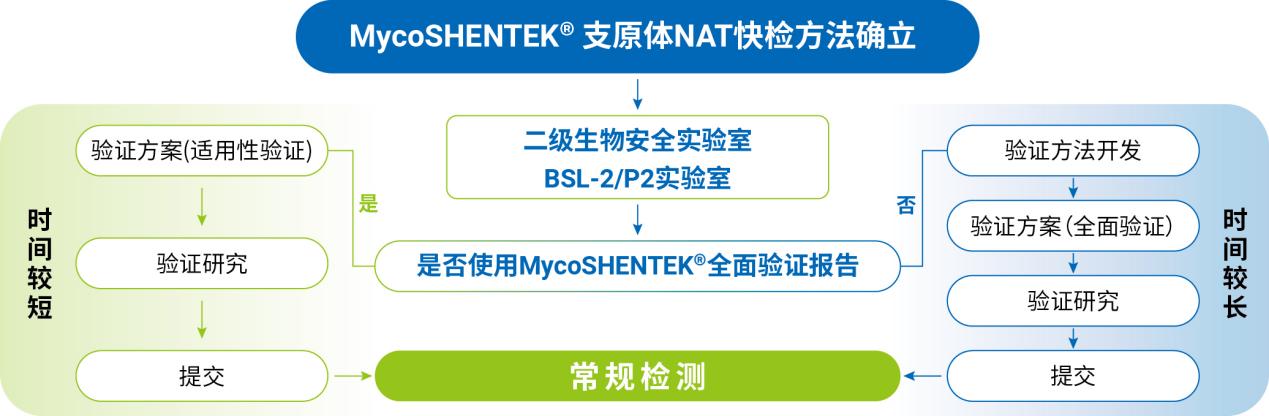
方法学验证服务:提供基于药典要求的完整验证方案支持和实验服务。
可比性研究:协助企业开展NAT法与传统培养法/指示细胞法的同步比对研究,这是方法替代的合规“通行证”。
五、总结
湖州申科生物技术股份有限公司的支原体qPCR检测解决方案,以经过严格三方验证的试剂盒为核心,以质量可控的标准品为基石,以全自动封闭检测系统为创新突破点,形成了覆盖“标准-试剂-设备-服务”的完整价值链。该体系不仅解决了传统检测周期长的核心痛点,更以强大的复杂基质耐受性应对新型生物制品的挑战,并前瞻性地符合全球最新、最严的法规要求(如EP 2026新规),为生物制药企业,尤其是CGT企业,实现从工艺监控到产品快速安全放行提供了可靠、合规、高效的一站式选择。



